Il Gruppo Chiesi annuncia che la Commissione europea ha approvato la modifica all’autorizzazione all’immissione in commercio per Trimbow® (beclometasone / formoterolo / glicopirronio), tripla terapia di combinazione fissa in formulazione extrafine in un singolo inalatore, come trattamento di mantenimento per pazienti adulti con asma non adeguatamente controllata con una combinazione di mantenimento di un beta2-agonista a lunga durata d’azione (LABA) e una dose media di corticosteroide per via inalatoria (ICS), che hanno manifestato una o più esacerbazioni dell’asma nell’anno precedente.
La decisione della Commissione si basa sul parere positivo del CHMP (Comitato per i Medicinali per uso umano) dell’EMA, espresso considerando i dati di efficacia e sicurezza di 4 studi clinici che hanno coinvolto quasi 3.000 pazienti.
Nei pazienti con asma non controllata, la tripla terapia di Chiesi ha mostrato una riduzione delle riacutizzazioni e un miglioramento della funzionalità polmonare rispetto all’ICS/LABA (corticosteroide inalatorio/β2-agonisti a lunga durata d’azione).
La tripla terapia in formulazione extrafine di Chiesi
La tripla terapia è una combinazione di:
- corticosteroide inalatorio (Inhaled Corticosteroid, ICS),
- β2-agonista a lunga durata d’azione (Long-Acting β2-Agonist, LABA),
- antagonista muscarinico a lunga durata di azione (Long-Acting Muscarinic Antagonist, LAMA).
Contiene infatti:
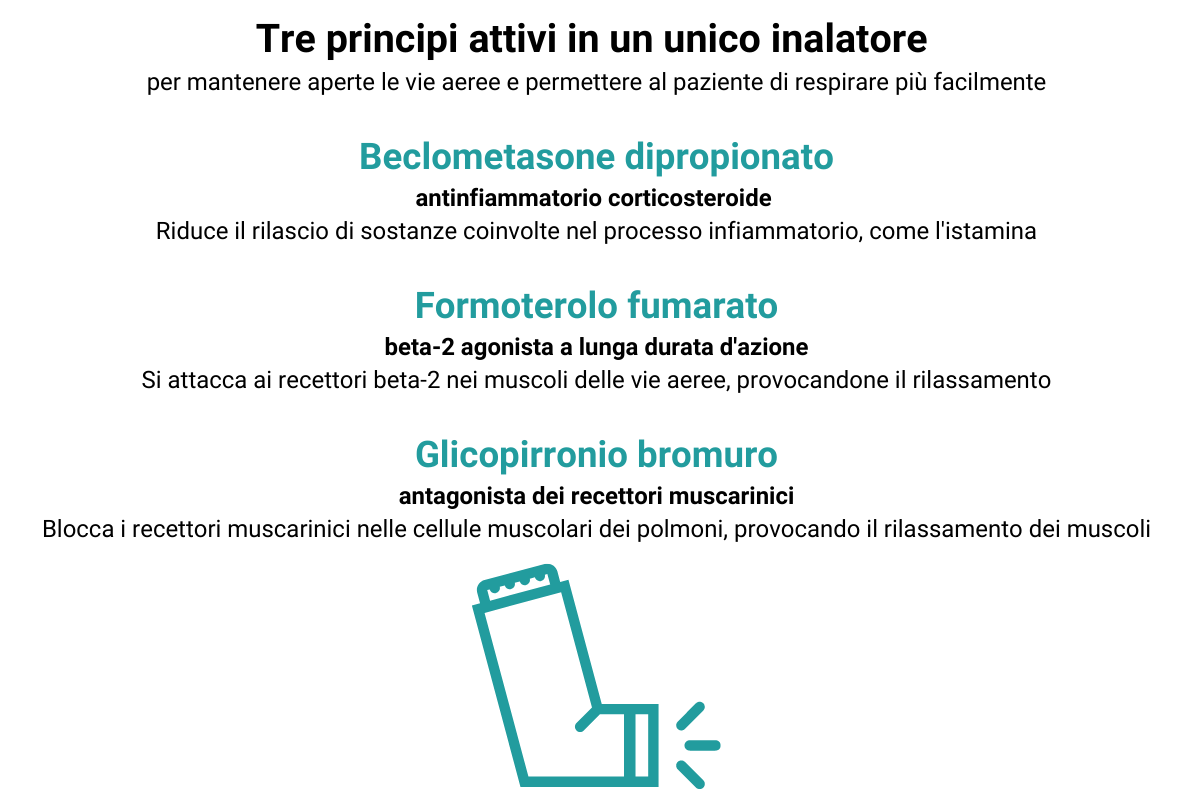
- beclometasone dipropionato (Beclometasone dipropionate, BDP; corticosteroide inalatorio) ICS,
- formoterolo fumarato (Formoterol fumarate, FF; agonista β2 a lunga durata d’azione) LABA,
- glicopirronio bromuro (Glycopyrronium, G; antagonista muscarinico a lunga durata d’azione) LAMA.
La tripla terapia di Chiesi in formulazione extrafine è in grado di raggiungere e trattare l’intero albero bronchiale, incluse le piccole vie aeree.
Sarà disponibile con una somministrazione due volte al giorno mediante un inalatore per soluzione pressurizzata. Il prodotto è dotato di un contatore di dosi che consente ai pazienti di monitorare e controllare l’avvenuta assunzione della terapia.
La tripla terapia di Chiesi, nel 2017, era stata approvata come terapia di mantenimento in pazienti adulti affetti da broncopneumopatia cronica ostruttiva (BPCO) da moderata a severa per i quali l’associazione di un corticosteroide inalatorio e un beta2-agonista a lunga durata d’azione o l’associazione di un beta2-agonista a lunga durata d’azione e un antagonista muscarinico a lunga durata d’azione non costituiscano un trattamento adeguato.


